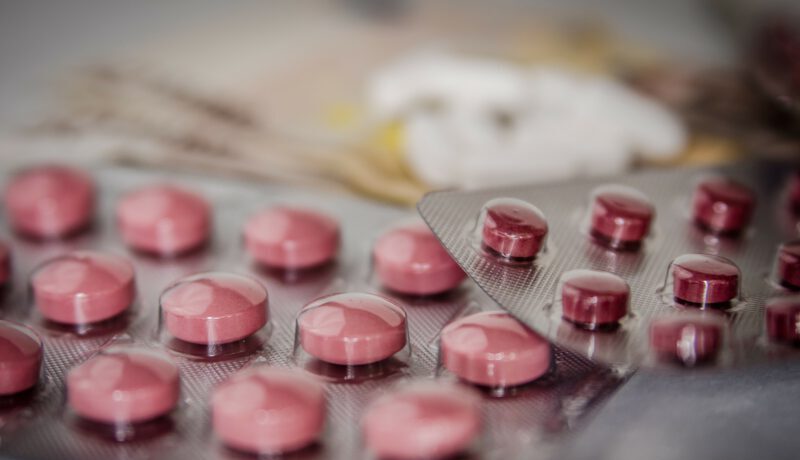
Władze Danii oficjalnie zatwierdziły sprzedaż leku firmy Merck & Co Inc., którego przyjmowanie ma prowadzić do ograniczania namnażania się koronawirusa. Molnupiravir będzie przeznaczony dla osób starszych i szczególnie narażonych na ciężkie przebycie choroby.
Jak wynika z informacji podawanych przez Reuters, Dania stała się pierwszym krajem w Unii Europejskiej, który oficjalnie zatwierdził sprzedaż i podawanie leku Molnupiravir. Pigułki wyprodukowane przez Merck & Co Inc. mają za zadanie ograniczać namnażanie się koronawirusa w organizmie zakażonego. Zdaniem ekspertów, lek ma wpłynąć na poważne ograniczenie liczby hospitalizowanych pacjentów. W pierwszych miesiącach preparat prawdopodobnie będzie przeznaczony jedynie dla osób starszych oraz tych będących w tzw. grupie ryzyka.
Ogłaszając zgodę na ograniczone stosowanie molnupiraviru w Danii, dyrektor medyczny Urzędu Zdrowia, Kirstine Moll Harboe, powiedziała: „Uważamy, że korzyści z leczenia z jego użyciem przeważają nad skutkami ubocznymi mogącymi wystąpić u tych pacjentów, którzy są najbardziej narażeni na poważne zachorowanie na COVID- 19”. Eksperci mają nadzieję, że zastosowanie leku w leczeniu znacząco zmniejszy liczbę osób, które będą wymagały hospitalizacji.
Wesprzyj nas już teraz!
Zanim molnupiravir trafił do obiegu, decyzję w sprawie stosowania leku wydała Europejska Agencja Leków. Zdecydowała wówczas, że dopuszcza preparat do stosowania i rekomenduje go pacjentom w pierwszych pięciu dniach przechodzenia choroby. Jednak jak wynika z informacji podawanych przez producenta, skuteczność leczenia molnupiravirem jest niższa niż zakładano. Pierwotnie lek miał ograniczać ryzyko hospitalizacji i zgonu o 50 proc., ale najnowsze badania wskazują na skuteczność leczenia na poziomie 30 proc.
Decyzją Europejskiej Agencji Leków, molnupiravir w Unii Europejskiej będzie oznaczony jako „Lagevrio”. Konkurencją dla tego preparatu może wkrótce zostać Paxlovid produkowany przez koncern Pfizer. Zdaniem ekspertów firmy produkującej tzw. szczepionki przeciwko Covid-19, lek ten ma zmniejszać ryzyko hospitalizacji lub śmierci aż o 89 procent. Preparat jest aktualnie badany przez amerykański organ regulacyjny, a do końca bieżącego roku, prawdopodobnie zostanie dopuszczony do użytku w USA.
Źródło: Reuters.com
WMa